RÉSUMÉ DES CARACTÉRISTIQUES DU PRODUIT
ANSM – Mis à jour le : 16/12/2020
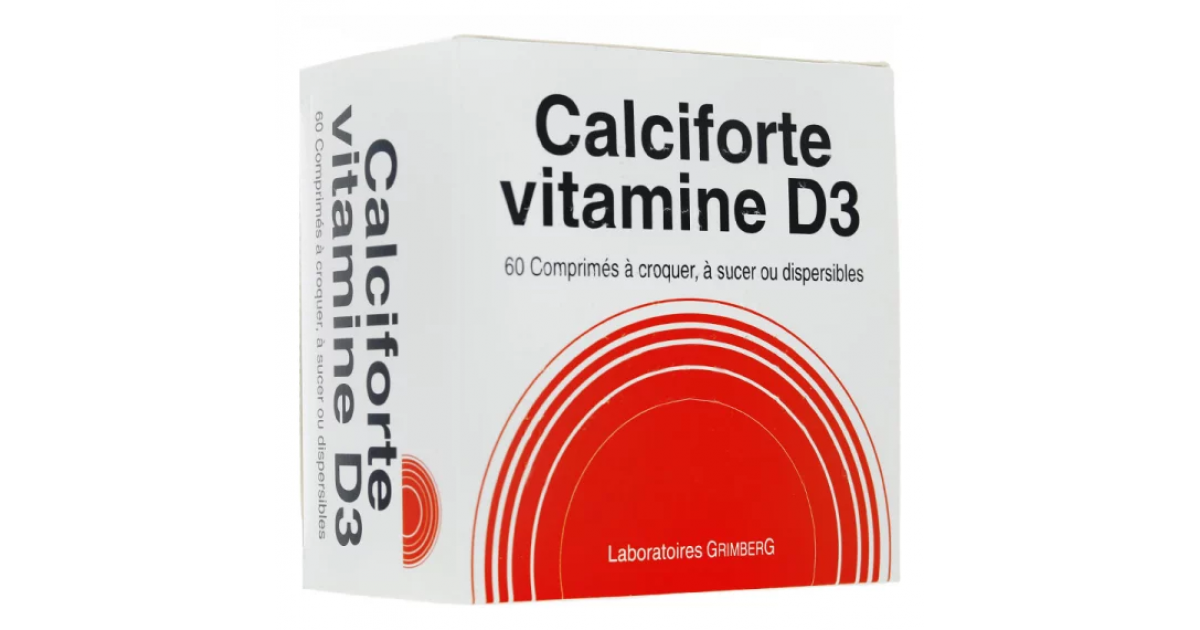
CALCIFORTE VITAMINE D3, comprimé à croquer, à sucer ou dispersible
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Calcium élément…………………………………………………………………………………………. 500,00 mg
Sous forme de carbonate de calcium………………………………………………………………. 1250,00 mg
Cholécalciférol ou vitamine D3……………………………………………………………………….400,00 UI
Sous forme de concentrat de cholécalciférol, forme pulvérulente
Levure Saccharomyces cerevisiae……………………………………………………………………… 50,00 mg
Pour un comprimé de 2,015 g.
Excipients à effet notoire : Aspartam, sorbitol, saccharose, protéines de soja
Pour la liste complète des excipients, voir rubrique 6.1.
Comprimé à croquer, à sucer ou dispersible.
4.1. Indications thérapeutiques
· Correction des carences vitamino-calciques chez les sujets âgés.
· Apport vitamino-calcique associé aux traitements spécifiques de l’ostéoporose, chez les patients carencés ou à haut risque de carence vitamino D-calcique.
4.2. Posologie et mode d’administration
Voie orale. Réservé à l’adulte.
La posologie quotidienne est de 2 comprimés par jour, soit 1 comprimé matin et soir.
Mode d’administration
Les comprimés sont à croquer, à sucer ou dispersibles.
Ce médicament est contre-indiqué en cas de :
· hypersensibilité aux substances actives ou à l’un des excipients mentionnés à la rubrique 6.1.
· hypercalcémie, hypercalciurie, lithiase calcique,
· immobilisation prolongée s’accompagnant d’hypercalciurie et/ou d’hypercalcémie : le traitement vitamino-calcique ne doit être utilisé qu’à la reprise de la mobilité,
· phénylcétonurie (en raison de la présence d’aspartam),
· allergie l’arachide ou au soja
4.4. Mises en garde spéciales et précautions d’emploi
Précautions d’emploi
· En cas de traitement de longue durée, il est justifié de contrôler la calciurie et de réduire ou d’interrompre momentanément le traitement si celle-ci dépasse 7,5 mmol/24 h (300 mg/24 h).
· En cas de traitement associé à base de cycline, de digoxine, de bisphosphonates, d’estramustine, de sels de fer, d’hormones thyroïdiennes, de strontium, de zinc, de rifampicine, de ciprofloxacine, de norfloxacine, d’inhibiteurs d’intégrase, d’anticonvulsivants inducteurs enzymatiques, d’orlistat et de diurétiques thiazidiques : voir Rubrique 4.5.
· Tenir compte de la dose de vitamine D par unité de prise (400 UI) et d’une éventuelle autre prescription de vitamine D. Ce produit contenant déjà de la vitamine D, l’administration supplémentaire de vitamine D ou de calcium doit être faite sous stricte surveillance médicale, avec contrôle hebdomadaire de la calcémie et de la calciurie.
· Le produit doit être prescrit avec précaution chez les patients atteints de sarcoïdose en raison d’une augmentation possible du métabolisme de la vitamine D en sa forme active. Chez ces patients, il faut surveiller la calcémie et la calciurie.
· Le produit doit être utilisé avec précaution chez les insuffisants rénaux avec surveillance du bilan phosphocalcique.
· Ce médicament contient 381,0 mg de sorbitol par comprimé. Les patients présentant une intolérance héréditaire au fructose (IHF) ne doivent pas prendre ou recevoir ce médicament.
· Ce médicament contient 10,0 mg d’aspartam par comprimé. L’aspartam contient une source de phénylalanine. Peut- être dangereux pour les personnes atteintes de phénylcétonurie.
· Ce médicament contient du saccharose. Les patients présentant une intolérance au fructose, un syndrome de malabsorption du glucose et du galactose ou un déficit en sucrase/isomaltase (maladie héréditaires rares) ne doivent pas prendre ce médicament.
· Ce médicament contient moins de 1 mmol (23 mg) de sodium par comprimé, c’est à dire qu’il est essentiellement « sans sodium ».
4.5. Interactions avec d’autres médicaments et autres formes d’interactions
Associations faisant l’objet de précautions d’emploi
+ Cyclines :
Diminution de l’absorption digestive des cyclines.
Prendre les sels de calcium à distance des cyclines (plus de 2 heures, si possible).
+ Digoxine :
Risque de troubles du rythme.
Surveillance clinique et, s’il y a lieu, contrôle de l’ECG et de la calcémie.
+ Bisphosphonates :
Risque de diminution de l’absorption digestive des bisphosphonates.
Prendre les sels de calcium à distance des bisphosphonates (de 30 minutes au minimum à plus de 2 heures, si possible, selon le bisphosphonate).
+ Estramustine :
Diminution de l’absorption digestive de l’estramustine.
Prendre les sels de calcium à distance de l’estramustine (plus de 2 heures, si possible).
+ Fer (sels) (voie orale) :
Diminution de l’absorption digestive des sels de fer.
Prendre le fer à distance des repas et en l’absence de calcium.
+Hormones thyroïdiennes :
Diminution de l’absorption digestive des hormones thyroïdiennes.
Prendre les sels de calcium à distance des hormones thyroïdiennes (plus de 2 heures, si possible).
+Strontium :
Avec les sels de calcium administrés par voie orale : diminution de l’absorption digestive du strontium.
Prendre le strontium à distance des sels de calcium (plus de 2 heures, si possible).
+ Zinc :
Diminution de l’absorption digestive du zinc par le calcium.
Prendre les sels de calcium à distance du zinc (plus de 2 heures, si possible).
+Rifampicine :
Diminution des concentrations de vitamine D plus marquée qu’en l’absence de traitement par rifampicine.
Dosage des concentrations de vitamine D et supplémentation si nécessaire.
+ Ciprofloxacine
Diminution de l’absorption digestive de la ciprofloxacine.
Prendre les sels de calcium à distance de la ciprofloxacine (plus de 2 heures, si possible).
+ Norfloxacine
Diminution de l’absorption digestive de la norflloxacine.
Prendre les sels de calcium à distance de la norfloxacine (plus de 2 heures, si possible).
+ Inhibiteurs d’intégrase
Diminution de l’absorption digestive des inhibiteurs d’intégrase.
Prendre les sels de calcium à distance de l’antirétroviral (plus de 2 heures, si possible).
+ Anticonvulsivants inducteurs enzymatiques :
Diminution des concentrations de vitamine D plus marquée qu’en l’absence de l’inducteur.
Dosage des concentrations de vitamine D et supplémentation si nécessaire.
Associations à prendre en compte
+ Diurétiques thiazidiques :
Risque d’hypercalcémie par diminution de l’élimination urinaire du calcium.
+ Orlistat :
Diminution de l’absorption de la vitamine D.
4.6. Fertilité, grossesse et allaitement
Grossesse
Ce médicament peut être utilisé pendant la grossesse. Cependant, la dose journalière ne doit pas dépasser 1500 mg de calcium et 600 UI de vitamine D3.
Pendant la grossesse, le surdosage en cholécalciférol doit être évité :
· des surdosages en vitamine D pendant la gestation ont eu des effets tératogènes chez l’animal.
· chez la femme enceinte, les surdosages en vitamine D doivent être évités car l’hypercalcémie permanente peut entraîner chez l’enfant un retard physique et mental, une sténose aortique supravalvulaire ou une rétinopathie. Cependant, plusieurs enfants sont nés sans malformation après administration de très fortes doses de vitamine D3 pour une hypoparathyroïdie chez la mère.
Ce médicament peut être utilisé pendant l’allaitement. Cependant, la dose journalière ne doit pas dépasser 1500 mg de calcium et 600 UI de vitamine D3.
· la vitamine D et ses métabolites passent dans le lait maternel.
4.7. Effets sur l’aptitude à conduire des véhicules et à utiliser des machines
· Constipation, flatulence, nausées, douleurs épigastriques, diarrhée ;
· Hypercalciurie et exceptionnellement hypercalcémie en cas de traitement prolongé à forte dose ;
· Prurit, rash cutané, urticaire ;
· Risque de survenue de réaction d’hypersensibilité (choc anaphylactique, urticaire), en raison de la présence de protéines de soja.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance – Site internet : www.signalement-sante.gouv.fr.
Le surdosage aigu se traduit par une hypercalciurie et une hypercalcémie dont les symptômes sont les suivants : nausées, vomissements, polydipsie, polyurie, constipation.
Un surdosage chronique en vitamine D3 peut provoquer des calcifications vasculaires et tissulaires en raison de l’hypercalcémie.
Traitement :
Arrêt de tout apport calcique et vitaminique D, réhydratation.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : SUPPLEMENTS MINERAUX
code ATC : A12AX
Mécanisme d’action
La vitamine D corrige l’insuffisance d’apport en vitamine D.
Elle augmente l’absorption intestinale du calcium et sa fixation sur le tissu ostéoïde.
L’apport de calcium corrige la carence calcique alimentaire.
Les besoins journaliers en calcium sont de l’ordre de 1000 à 1500 mg de calcium élément et 500 à 1000 UI/jour de vitamine D.
La vitamine D et le calcium corrigent l’hyperparathyroïdie sénile secondaire.
Efficacité et sécurité clinique
Une étude contrôlée, en double aveugle, contre placebo de 18 mois, portant sur 3270 femmes âgées de 84 ± 6 ans vivant dans des centres de soins, a montré une diminution significative des taux plasmatiques de PTH. A 18 mois, les résultats de l’analyse en intention de traitement ont révélé 80 fractures de hanche dans le groupe calcium-vitamine D et 110 fractures de hanche dans le groupe placebo (p = 0,004).
Dans les conditions de cette étude, le traitement de 1387 femmes a empêché 30 fractures de hanche. Après une prolongation jusqu’à 36 mois, les résultats suivants ont été obtenus : 137 fractures de hanche dans le groupe calcium-vitamine D et 178 dans le groupe placebo (p £0,02).
5.2. Propriétés pharmacocinétiques
Carbonate de calcium
En milieu gastrique, le carbonate de calcium libère l’ion calcium, en fonction du pH.
Le calcium est essentiellement absorbé dans la partie haute de l’intestin grêle.
Le taux d’absorption par voie gastro-intestinale est de l’ordre de 30 pour cent de la dose ingérée.
Le calcium est éliminé par la sueur et les sécrétions digestives.
Le calcium urinaire dépend de la filtration glomérulaire et du taux de réabsorption tubulaire du calcium.
Vitamine D3
La vitamine D3 est absorbée dans l’intestin et transportée par liaisons protéiques dans le sang jusqu’au foie (première hydroxylation) et au rein (deuxième hydroxylation).
La vitamine D3 non hydroxylée est stockée dans les compartiments de réserve tels que les tissus adipeux et musculaires.
Sa demi-vie plasmatique est de l’ordre de quelques jours. Elle est éliminée dans les fèces et les urines.
5.3. Données de sécurité préclinique
Amidon prégélatinisé, sorbitol, dibéhénate de glycérol, croscarmellose sodique, aspartam, arôme orange poudre (maltodextrine, protéines de soja, gomme arabique, jus concentré d’orange, huile essentielle d’orange, huile essentielle de citron, citral, aldéhyde acétique, linalol, butyrate d’éthyle, alpha terpinéol, octanal, acétate d’éthyle, acétate de géranyle).
Enrobage du concentrat de cholécalciférol : alpha-tocophérol, graisses alimentaires, gélatine, saccharose, amidon de maïs.
2 ans.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas + 25°C
6.5. Nature et contenu de l’emballage extérieur
Comprimés sous plaquettes (PVC/PVDC/Aluminium). Boîte de 60 ou 180.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
44 AVENUE GEORGES POMPIDOU
92300 LEVALLOIS-PERRET
FRANCE
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 356 682 5 7 : 60 comprimés sous plaquettes (PVC/PVDC/Aluminium)
· 34009 373 774 1 6 : 180 comprimés sous plaquettes (PVC/PVDC/Aluminium)
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Médicament non soumis à prescription médicale.