Clavicin® injectable
1. Dénomination du médicament
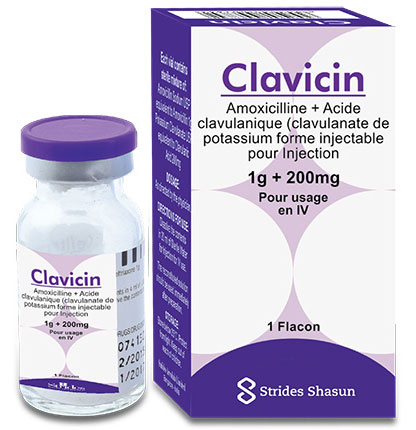
Clavicin® injectable.
2. Composition qualitative et quantitative
Chaque flacon contient :
- un mélange stérile d’amoxicilline sodique USP équivalent à amoxicilline 1 g ;
- et de clavulanate de potassium USP équivalent à acide clavulanique 200 mg.
3 – Forme pharmaceutique
Mélange stérile pour injection en flacon.
4. Données cliniques
4.1 Indications thérapeutiques
Clavicin® est indiqué chez l’adulte et l’enfant dans le traitement des infections suivantes :
- Infections graves de la sphère ORL (par ex.: mastoïdite, infections péri-amygdaliennes, épiglottites, et sinusites lorsqu’elles sont associées à des signes généraux graves) ;
- exacerbations aiguës de bronchite chronique, (diagnostic bien posé) ;
- pneumonie communautaire acquise ;
- cystite ;
- pyélonéphrite ;
- infections de la peau et du tissu sous-cutané (en particulier la cellulite) ;
- morsures d’animaux ;
- abcès dentaires graves associé à une cellulite évolutive ;
- infections osseuses et articulaires, l’ostéomyélite en particulier ;
- infections intra-abdominales ;
- infections génitales de la femme ;
- Prophylaxie des infections chirurgicales chez l’adulte, notamment les chirurgies lourdes impliquant le tube digestif, la cavité pelvienne, la tête et le cou, la chirurgie biliaire.
Prendre en compte les directives nationales de bonne pratique d’utilisation des antibiotiques.
4.2. Posologie et mode d’administration
La posologie de Clavicin® doit être adaptée à chaque patient, et doit prendre en compte : les germes suspectés et leur sensibilité aux antibiotiques, la sévérité et le site de l’infection, l’âge, le poids et le statut rénal du patient.
Adultes et enfants ≥ 40 kg
La posologie est de 1000 mg/ 200 mg toutes les 8 heures.
Enfants < 40 kg
Enfants à partir de 3 mois : 25 mg/5 mg par kg toutes les 8 heures.
Personnes âgées
Pas d’ajustement posologique nécessaire.
Insuffisance rénale
La dose doit être ajustée en tenant compte de la dose maximale d’amoxicilline recommandée. Pas d’ajustement posologique nécessaire chez les patients ayant une clairance de la créatinine ClCr supérieure à 30 ml/min.
Insuffisance hépatique
La dose doit être adaptée avec précaution. La fonction hépatique doit être évaluée à intervalles réguliers.
4.3. Contre-indications
- Hypersensibiliré ;
- antécédent d’ictère / insuffisance hépatique impliquant l’amoxicilline/acide clavulanique.
4.4. Mises en garde et précautions d’emploi
Antécédent d’allergie à la pénicilline, patients atopiques, signes présomptifs de mononucléose infectieuse, insuffisance hépatique.
4.5. Grossesse et allaitement
Grossesse
Les données sur l’utilisation de l’amoxicilline/acide clavulanique chez la femme enceinte sont limitées et n’indiquent pas une augmentation du risque de malformations congénitales. Sauf avis contraire du médecin, ce médicament ne doit pas être utilisé au cours de la grossesse.
Allaitement
L’amoxicilline/acide clavulanique ne doit être utilisé chez la femme allaitante qu’après évaluation rigoureuse du rapport bénéfice/risque par le médecin.
4.6 Effets indésirables
Les effets indésirables les plus fréquemment rapportés sont : diarrhée, nausées et vomissements.
5. Données pharmaceutiques
5.1. Classe pharmacothérapeutique
Antibactériens. Code ATC : J01CR02
5.2. Nature et contenu de l’emballage extérieur
Boîte de 1 flacon de mélange stérile.
6 – Conditions de prescription et de délivrance
Liste I
7 – Titulaire de l’AMM
Strides Pharma Science Limited
Strides House, Opp IIM-B, Bilekahalli,
Bannerghatta Road,
Bangalore – 560076, India
8 – Date de mise à jour du texte
Février 2019.
Dernière mise à jour de cette page
04/06/2019.