Introduction
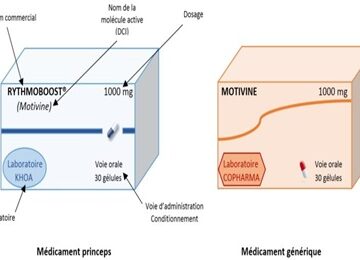
Les médicaments génériques sont des copies de médicaments originaux (princeps) dont le brevet est expiré. Ils contiennent les mêmes principes actifs, dosages, formes pharmaceutiques et voies d’administration que les médicaments de référence, et doivent démontrer leur bioéquivalence pour être approuvés. Selon l’Organisation mondiale de la Santé (OMS), les médicaments génériques peuvent coûter jusqu’à 60-80 % moins cher que les médicaments originaux tout en conservant la même efficacité (WHO, 2021).
Dans les pays développés, les génériques représentent une part importante des traitements dispensés : plus de 80 % aux États-Unis par exemple (Saha et al., 2022). En Afrique, le taux de recours reste plus faible en raison de nombreux défis : manque de sensibilisation, faibles capacités de production locale, méfiance des patients, etc. Au Cameroun, bien que le ministère de la Santé publique encourage leur utilisation, la part des médicaments génériques sur le marché reste marginale (Ngono et al., 2020).
Pourquoi les Médicaments Génériques sont Essentiels
Les médicaments génériques jouent un rôle essentiel dans les systèmes de santé, surtout dans les pays à revenu faible ou intermédiaire. Ils contribuent à :
-
Réduire le coût des soins de santé pour les patients et les systèmes nationaux (Kesselheim et al., 2008).
-
Améliorer l’accès aux traitements pour les maladies chroniques comme l’hypertension, le diabète ou le VIH/SIDA.
-
Soutenir la couverture santé universelle, un objectif de l’OMS.
Qualité, Efficacité et Bioéquivalence
Contrairement à certaines idées reçues, les médicaments génériques sont soumis à des exigences strictes. Les autorités sanitaires comme l’OMS, la FDA (USA) ou l’EMA (Europe) exigent des preuves de bioéquivalence, c’est-à-dire une similarité dans la vitesse et la quantité de principe actif absorbé (WHO, 2018). Ils doivent aussi répondre aux normes de Bonnes Pratiques de Fabrication (BPF).
Situation au Cameroun
Au Cameroun, l’accès aux médicaments reste un défi. Environ 60 % de la population se procure ses médicaments hors du circuit réglementé, notamment dans la rue, ce qui expose à des produits contrefaits ou inefficaces. Le gouvernement promeut les génériques à travers des politiques de santé publique et la promotion de la pharmacovigilance (MINSANTE, 2022).
Sur MboaPharma.cm, les utilisateurs peuvent consulter les prix des médicaments génériques, leur disponibilité dans les pharmacies locales, accéder aux pharmacies de garde et éviter les achats dans la rue.
Défis et Solutions pour Favoriser leur Adoption
Défis :
-
Méfiance du public face à la qualité des génériques.
-
Manque de campagnes de sensibilisation.
-
Absence de politique de substitution automatique par les pharmaciens.
Solutions :
-
Formation des professionnels de santé.
-
Communication publique sur l’efficacité des génériques.
-
Encourager la production locale sous licence.
Enjeux pour l’Avenir
D’ici 2030, l’OMS vise à ce que tous les pays adoptent des politiques solides sur les médicaments génériques. Pour le Cameroun, cela passe par :
-
La lutte contre les médicaments falsifiés.
-
La réglementation des circuits de distribution.
-
L’amélioration de la confiance des patients.
Consultez gratuitement la disponibilité des médicaments génériques sur MboaPharma.cm et évitez les achats risqués dans la rue !
Vous pouvez également consulter notre article sur Génériques Vs Princeps : Quelle Différence Et Comment Choisir ?
Foire aux questions (FAQ)
Les médicaments génériques sont-ils aussi efficaces que les originaux ?
Oui, ils ont la même composition, même effet thérapeutique et sont approuvés par les autorités sanitaires.
Peut-on faire confiance aux médicaments génériques au Cameroun ?
Oui, s’ils sont achetés en pharmacie ou sur des plateformes fiables comme MboaPharma.cm.
Pourquoi sont-ils moins chers ?
Parce qu’ils ne supportent plus les coûts de recherche et de marketing du médicament original.
Sont-ils disponibles dans toutes les pharmacies ?
Non, mais vous pouvez vérifier leur disponibilité en temps réel sur MboaPharma.cm.
Références scientifiques
-
WHO (2021). Generic medicines. https://www.who.int/news-room/fact-sheets/detail/generic-medicines
-
Saha, S. et al. (2022). Trends in Generic Drug Use. PubMed. https://pubmed.ncbi.nlm.nih.gov/35250997
-
Kesselheim, A. S. et al. (2008). Clinical equivalence of generic and brand-name drugs. JAMA. https://jamanetwork.com/journals/jama/fullarticle/182694
-
WHO (2018). Bioequivalence studies in the WHO prequalification of medicines programme. https://www.who.int/docs/default-source/medicines/norms-and-standards/bioequivalence.pdf
-
Ngono, E. et al. (2020). Access to Essential Medicines in Cameroon. NIH. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7334569
-
MINSANTE (2022). Politique Nationale Pharmaceutique du Cameroun. http://www.minsante.cm

I don’t think the title of your article matches the content lol. Just kidding, mainly because I had some doubts after reading the article. https://accounts.binance.com/en-NG/register-person?ref=YY80CKRN
Your point of view caught my eye and was very interesting. Thanks. I have a question for you.